引言
最常见的酶动力学实验是改变底物浓度并测量酶速率。其目的是确定酶的Km值(产生半最大速率的底物浓度)和Vmax值(最大速率)。如果您的目标是确定周转数kcat,而不是Vmax,请使用该方程的另一种形式。
分步操作
创建一个XY数据表。将底物浓度输入X列,酶速率输入Y列。如果有多个实验条件,请将第一个条件放在A列,第二个放在B列,依此类推。
您也可以选择 Prism 的示例数据:酶动力学 - 米氏-门捷列夫模型。
输入数据后,点击“分析”,选择“非线性回归”,选择“酶动力学方程”面板,并选择“米氏-门捷列夫酶动力学”。
模型
Y = Vmax*X/(Km + X)
参数解读
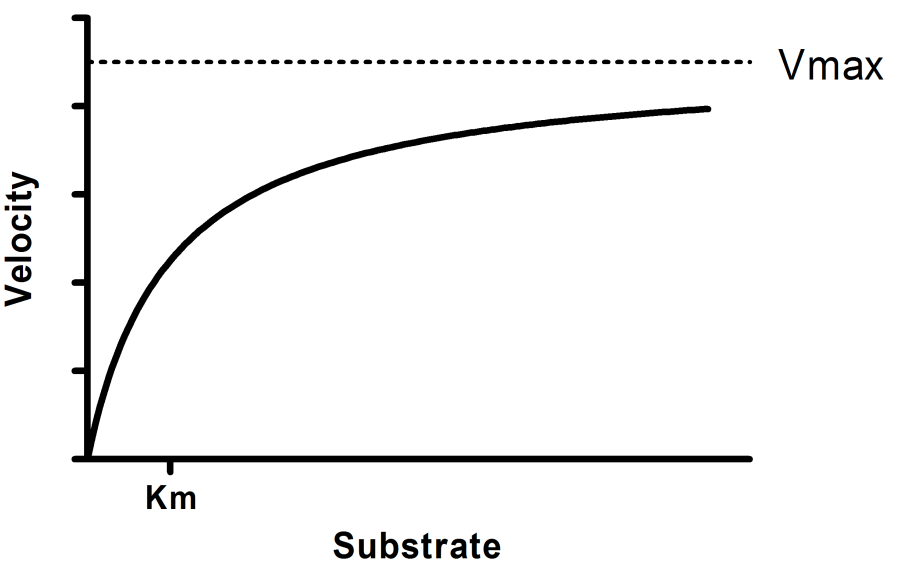
Vmax 是最大酶速率,单位与 Y 相同。它是酶在极高底物浓度下外推得到的速率,因此其值几乎总是高于实验中测得的任何速率。
Km 是米氏-门登常数,单位与 X 相同。它是达到半最大酶速率所需的底物浓度。
绘制 Lineweaver-Burk 图
在非线性回归技术出现之前,研究者必须将曲线数据转换为直线,以便进行线性回归分析。实现这一目标的一种方法是绘制莱纳韦弗-伯克图,该图以底物浓度的倒数为横轴,酶速率的倒数为纵轴。
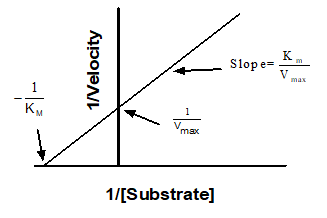
若绘制了 Lineweaver-Burk 图,请仅将其用于展示数据。 切勿利用线性回归直线的斜率和截距来确定 Vmax 和 Km 的数值。若采用此方法,将无法获得最精确的 Vmax 和 Km 值。问题在于,这些转换(倒数运算)会扭曲实验误差,因此双倒数图不符合线性回归的假设条件。请使用非线性回归来获取最精确的 Km 和 Vmax 值。
要创建 Lineweaver-Burk 图(含对应直线),首先需记录非线性回归报告的 Vmax 和 Km 数值(后续会用到)。首先,在包含数据的数据表中,点击工具栏中的“分析”按钮,从“转换、归一化...”分析选项中选择“转换”,然后点击“确定”。 在“函数列表”下拉菜单中,选择“药理学和生物化学转换”。选择“Lineweaver-Burk”选项并点击“确定”(请确保已勾选“为结果创建新图表”复选框)。
现在,我们需要在 Lineweaver-Burk 图中添加相应的直线。请勿直接执行线性回归,因为如上所述,这将无法生成正确的直线。请按照以下步骤操作:
1.在转换后数据的图表中,点击工具栏“分析”区域中的“分析”按钮
2.在“生成曲线”分析部分中选择“绘制函数”,然后点击“确定”
3.在弹出的对话框中,于“函数”选项卡的函数列表中选择“直线”
4.使用“函数”选项卡底部的“X 值范围”选项来指定直线的起始点和终点
5.切换至“参数值与列标题”选项卡
6.计算 1/Vmax 并将其作为 Y 截距输入(其中 Vmax 是之前非线性回归报告的值)
7.将 Km/Vmax 输入为斜率(其中 Km 和 Vmax 是先前非线性回归报告的数值)
8.点击“确定”
9.Prism 将生成一个名为“绘制函数”的新数据表。点击并拖动该表至 Lineweaver-Burk 图上,然后点击“添加”
注释
•参见所有酶动力学分析的假设列表。
•该方程拟合的曲线与拟合转数 Kcat 而不是 Vmax 的方程完全相同。Kcat 与 Et(酶位点浓度)的乘积等于 Vmax,因此,如果已知 Et,Prism 即可拟合 Kcat。
•
•请注意,Km 并非衡量酶与底物结合强度的结合常数。其数值既考虑了底物对酶的亲和力,也考虑了结合在酶上的底物转化为产物的速率。