引言
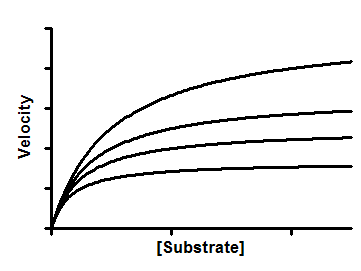
非竞争性抑制剂会与酶-底物复合物结合,但不会与游离酶结合。这会同时降低有效Vmax和有效Km。底物-速率曲线向下并向左平移。
可以通过在不同浓度的抑制剂存在下测定底物-速率曲线,来确定竞争性抑制剂的Ki值。
分步操作
创建一个 XY 数据表。在 X列中输入底物浓度,在 Y列中输入酶活性。每个数据集(Y列)代表在不同浓度抑制剂存在下收集的数据,从零开始。将这些浓度输入到列标题中。请确保输入的是浓度,而不是浓度的对数。
输入数据后,点击“分析”,选择“非线性回归”,选择“酶动力学方程”面板,并选择“非竞争性酶抑制”。
模型
VmaxApp=Vmax/(1+I/AlphaKi)
KmApp=Km/(1+I/AlphaKi)
Y=VmaxApp*X/(Kmapp+X)
常数 I 代表抑制剂浓度,该值需输入到各列标题中。此值受限于必须等于数据集中的某个常数。
参数 Vmax、Km 和 Ki 是共享的,因此 Prism 会为整个数据集拟合一个控制数据。
参数解读
Vmax 是无抑制剂条件下的最大酶速率,其单位与 Y 相同。
Km 是米氏常数(无抑制剂条件下),其单位与 X 相同。它描述了无抑制剂条件下底物与酶的交互作用。
AlphaKi 是抑制常数,其单位与您在列标题中输入的 I 相同。它是 Ki(由于非竞争性抑制剂不与酶结合,因此该值非常高)与 alpha(该值非常低)的乘积。无法分别拟合 alpha 和 Ki,只能确定它们的乘积。有些书籍将此乘积称为 Ki'。
如果数据与该模型拟合不佳,请考虑改用竞争性或非竞争性模型进行拟合。或者采用混合模型抑制的更通用方程进行拟合。
参考文献
方程 3.6 出自:RA Copeland,《药物发现中的酶抑制剂评估》,Wiley 2005。ISBN:0471686964。RA Copeland,《药物发现中的酶抑制剂评估》,Wiley 2005。ISBN:0471686964。