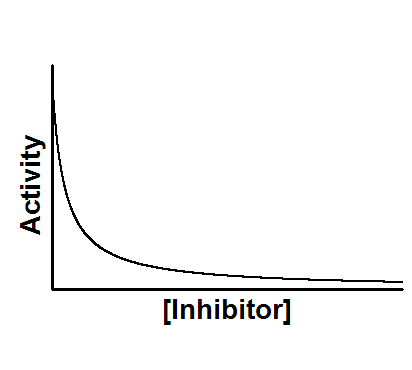
引言
该方程考虑了强结合效应,因此不假设抑制剂的游离浓度等于总浓度。
分步操作
创建一个 XY 数据表。在 X列中输入抑制剂浓度(通常以微摩尔为单位,但任何浓度单位均可),在 Y 列中输入酶活性(任何单位均可)。如果有多个实验条件,请将第一个放入 A 列,第二个放入 B 列,依此类推。
输入数据后,点击“分析”,选择“非线性回归”,选择“酶动力学方程”面板,并选择“Morrison Ki”。
将 Et、S 和 Km 约束为常数值
您必须将三个参数约束为常数值。要进行约束,请转至非线性回归对话框的“约束”选项卡,确保 Et、S 和 Km 旁边的下拉菜单设置为“等于常数”,并输入相应数值。
•Et 是酶催化位点的浓度,其单位应与 X 值一致。如果酶具有多个亚基,请注意 Et 表示催化位点的浓度,该值可能大于酶分子的浓度。
•S 是您选择使用的底物浓度。请使用与 X 值相同的单位。
•Km 是米氏常数,单位与 X 相同,需在无竞争剂的实验中测定。
Prism无法从活性与抑制剂浓度关系图中拟合出这些参数。您必须根据实验设计已知S值,通过其他实验确定Km和Et,并将这三者均设为常量。
模型
Q=(Ki*(1+(S/Km)))
Y=Vo*(1-((((Et+X+Q)-(((Et+X+Q)^2)-4*Et*X)^0.5))/(2*Et)))
参数解读
V0 是无抑制剂条件下的酶速率,单位与 Y 相同。这与 Vmax 不同,后者需要底物浓度达到最大值。
Ki 是抑制常数,其单位与 X 相同。
IC50 与 Ki(Kusmic)不同。实际上,IC50 = Et/2 + Ki
参考文献
方程 9.6,见 RA Copeland,《酶》,第 2 版,Wiley,2000 年。
Petr Kuzmic,《为何 IC50 值对您不利及其他意外发现》